SLC转运蛋白敲除细胞:从代谢调控到药物靶点发现

溶质载体(Solute Carrier,SLC)超家族是人体最大的跨膜转运蛋白家族,编码基因约占人类蛋白编码基因组的5.2%。从葡萄糖、氨基酸到药物分子,SLC负责调控几乎所有生命必需物质的跨膜运输。
01
为什么SLC是值得关注的新兴靶点家族?
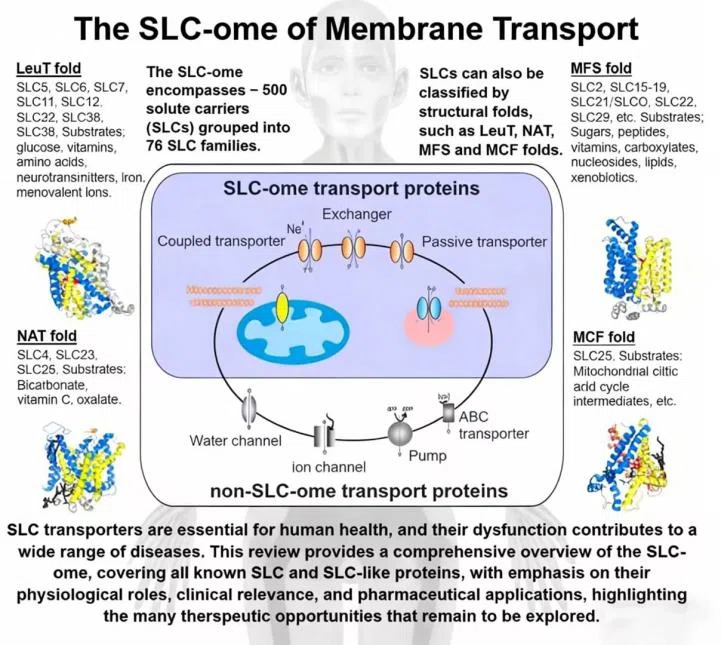
SLC超家族包含约460个成员,分布于76个家族,另有52个SLC样蛋白,总数达516个。它们不仅是营养物质进出细胞的“看门人”,其功能异常还直接参与多种重大疾病的发生发展。
·肿瘤代谢:GLUT1、LAT1、ASCT2、xCT等SLC成员驱动肿瘤代谢重编程,选择性抑制剂已进入临床前研究。
·心血管与代谢疾病:SLC2A家族与糖尿病相关;SLC22A家族(OATs、OCTs)参与药物及代谢物转运,影响血压、血脂。
·神经退行性疾病:SLC1A2(GLT-1)功能障碍与肌萎缩侧索硬化(ALS)有关;SLC6A4(SERT)与抑郁症相关。
·药物ADME:OAT1(SLC22A6)、OCT2(SLC22A2)等决定药物在肾脏的清除速率,影响药效与毒性。
·肿瘤代谢:GLUT1、LAT1、ASCT2、xCT等SLC成员驱动肿瘤代谢重编程,选择性抑制剂已进入临床前研究。
·心血管与代谢疾病:SLC2A家族与糖尿病相关;SLC22A家族(OATs、OCTs)参与药物及代谢物转运,影响血压、血脂。
·神经退行性疾病:SLC1A2(GLT-1)功能障碍与肌萎缩侧索硬化(ALS)有关;SLC6A4(SERT)与抑郁症相关。
·药物ADME:OAT1(SLC22A6)、OCT2(SLC22A2)等决定药物在肾脏的清除速率,影响药效与毒性。

02
为什么SLC基因编辑细胞是功能研究的“利器”?
CRISPR/Cas9介导的基因敲除可在基因组水平实现目标基因的完全功能丧失,具有以下不可替代的优势:
·完全功能缺失:敲除导致蛋白完全失活,表型明确,可重复性高。
·稳定遗传:单克隆细胞株可长期传代,无需重复转染。
·适用于高通量筛选:可用于构建SLC家族敲除文库,进行系统性的遗传互作分析。
2025年发表于《Molecular Systems Biology》的研究利用CRISPR系统对人类SLC超家族进行了大规模遗传互作图谱绘制,筛选了35421对SLC-SLC双重敲除组合,发现细胞转运系统表现出显著的代谢冗余和韧性,仅有0.67%的SLC-SLC基因对显示出遗传相互作用。
这一发现提示,靶向单个SLC可能不足以产生显著表型,需结合组合敲除或功能协同分析。
除了敲除策略,点突变模型是解析SLC功能的另一重要工具。许多疾病相关的SLC突变是错义突变(单个氨基酸替换),而非功能完全丧失。通过CRISPR介导的精准点突变,可以:
· 模拟人类遗传病中的特定SLC错义突变
· 研究关键氨基酸残基对转运活性、底物选择性的影响
· 筛选靶向突变体的特异性抑制剂
03
SLC敲除细胞在转化研究中的代表性应用
1. SLC38A1:MDS/AML中的代谢治疗新靶点
SLC38A1是一种非经典的谷氨酰胺转运蛋白。
2025年AACR年会上报道的研究发现,SLC38A1在高危骨髓增生异常综合征(MDS)和急性髓系白血病(AML)患者的长期造血干细胞中显著过表达,且与患者总生存期缩短相关。
利用CRISPR介导的SLC38A1敲除,研究者证实:在MOLM13、THP-1和MDS-L细胞中,存活集落分别减少37%、42%和43%。在原代AML及高危MDS患者样本中,敲除同样有效抑制细胞活力和集落形成能力。
这一研究提示,靶向SLC38A1的代谢干预策略有望为MDS/AML患者带来新的治疗选择。
2. SLC22A6(OAT1):肾脏药物转运的经典模型
有机阴离子转运蛋白1(OAT1/SLC22A6)在肾脏近端小管细胞中表达,介导抗病毒药、抗生素、利尿剂等大量临床药物的摄取。OAT1的功能缺失可导致药物清除率下降,增加毒性风险。
利用SLC22A6敲除细胞模型,可以评估候选化合物是否为OAT1底物,预测药物-药物相互作用,筛选低肾毒性的新分子实体。
3. SLC35A1:病毒受体与基因治疗工具
SLC35A1编码CMP-唾液酸转运蛋白,负责细胞表面糖蛋白的唾液酸化,是流感病毒、副流感病毒等多种病毒进入宿主细胞的关键受体。
全基因组CRISPR筛选证实,SLC35A1敲除可显著抑制病毒复制。此外,在HEK293T和HeLa细胞中敲除SLC35A1可提高AAV9的转导效率,为基因治疗效力检测提供了优化工具。
04
如何高效开展SLC功能研究?——现货SLC敲除/点突变细胞库
面对SLC家族数百个成员,逐个构建敲除细胞周期长、成本高。艾迪基因提供现货SLC基因编辑细胞,覆盖多个研究热门的转运蛋白靶点,帮助您将精力集中于核心科学问题。
产品优势
·基于CRISPR/Cas9技术构建,单克隆保证,Sanger测序验证敲除。
·现货供应,即订即发,节省2-3个月的建系时间。
·多种细胞背景可选:HEK293、HeLa、Huh-7、HCT116等。
·附带验证数据:提供测序峰图。
部分现货SLC敲除细胞列表
更多SLC家族敲除细胞(钠、钾、钙离子通道等)及定制服务,请联系艾迪基因客服
05
结语
SLC转运蛋白家族正从基础研究的“配角”走向药物靶点发现的“主角”。无论是探索肿瘤代谢重编程、解析药物转运机制,还是开发新的治疗策略,SLC敲除细胞模型都是不可或缺的核心工具。
艾迪基因现货SLC敲除细胞库,以专业的技术、可靠的验证、快速的交付,助力您的科研每一步。
参考文献
1. Gyimesi, G., et al. (2025). The SLC-ome of membrane transport: From molecular discovery to physiology and clinical applications. Physiological Reviews. Advance online publication.
2. Alam, S., et al. (2023). Membrane transporters in cell physiology, cancer metabolism and drug response. Disease Models & Mechanisms, 16(11), dmm050404.
3. Gou, X., et al. (2022). Construction and evaluation of a novel organic anion transporter 1/3 CRISPR/Cas9 double-knockout rat model. Pharmaceutics, 14(11), 2307.
4. 4.Girardi, E., et al. (2020). A widespread role for SLC transmembrane transporters in resistance to cytotoxic drugs. Nature Chemical Biology, 16(4), 469–478.

2. Alam, S., et al. (2023). Membrane transporters in cell physiology, cancer metabolism and drug response. Disease Models & Mechanisms, 16(11), dmm050404.
3. Gou, X., et al. (2022). Construction and evaluation of a novel organic anion transporter 1/3 CRISPR/Cas9 double-knockout rat model. Pharmaceutics, 14(11), 2307.
4. 4.Girardi, E., et al. (2020). A widespread role for SLC transmembrane transporters in resistance to cytotoxic drugs. Nature Chemical Biology, 16(4), 469–478.

联系我们
18102225074(微信同号)market@edgene.cn