VEGF信号通路敲除细胞系|血管生成研究模型

01
VEGF信号通路概述
VEGF Signaling Pathway是血管生成的关键调控机制,对生理和病理状态至关重要。其中,VEGF信号通路通过调控内皮细胞(EC)的增殖、迁移和存活,从而促进新生血管的有序发育。
VEGF家族包含多种配体,其中以VEGF-A在血管生成中的作用最为突出。
VEGF-A 通过外显子选择性剪接产生多种异构体,例如:
l VEGF-A165是最常见的可溶性/肝素结合型异构体,具有强促血管生成活性;VEGF-A121扩散能力强但活性较低;VEGF-A189高度结合细胞外基质,形成浓度梯度;
l VEGF-B和PlGF主要结合VEGFR-1,参与组织代谢保护和病理性血管生成;
l VEGF-C和VEGF-D 以前体形式存在,经蛋白酶(如furin、ADAMTS3、纤溶酶)加工成熟后,主要促进淋巴管生成,也可激活血管生成;
l PlGF 可与VEGF-A形成异源二聚体,增强信号强度。
这些配体异构体的差异化表达和结合特性,共同决定了VEGF信号的时空特异性,从而精细调控血管生成的效率、稳定性和功能完整性。
VEGF家族包含多种配体,其中以VEGF-A在血管生成中的作用最为突出。
VEGF-A 通过外显子选择性剪接产生多种异构体,例如:
l VEGF-A165是最常见的可溶性/肝素结合型异构体,具有强促血管生成活性;VEGF-A121扩散能力强但活性较低;VEGF-A189高度结合细胞外基质,形成浓度梯度;
l VEGF-B和PlGF主要结合VEGFR-1,参与组织代谢保护和病理性血管生成;
l VEGF-C和VEGF-D 以前体形式存在,经蛋白酶(如furin、ADAMTS3、纤溶酶)加工成熟后,主要促进淋巴管生成,也可激活血管生成;
l PlGF 可与VEGF-A形成异源二聚体,增强信号强度。
这些配体异构体的差异化表达和结合特性,共同决定了VEGF信号的时空特异性,从而精细调控血管生成的效率、稳定性和功能完整性。
02
下游信号传导机制
它们主要通过结合并激活跨膜受体酪氨酸激酶——尤其是VEGFR-2(KDR/Flk-1)——启动下游信号传导。
在信号传导过程中,多个经典通路被协同激活:
l PI3K/AKT通路:主要负责促进内皮细胞存活、抑制凋亡,并通过eNOS激活增强血管稳定性与通透性调控;
l 此外,PLCγ-PKC 通路调控钙离子释放和通透性,Src/FAK 通路促进细胞骨架重排与迁移。
03
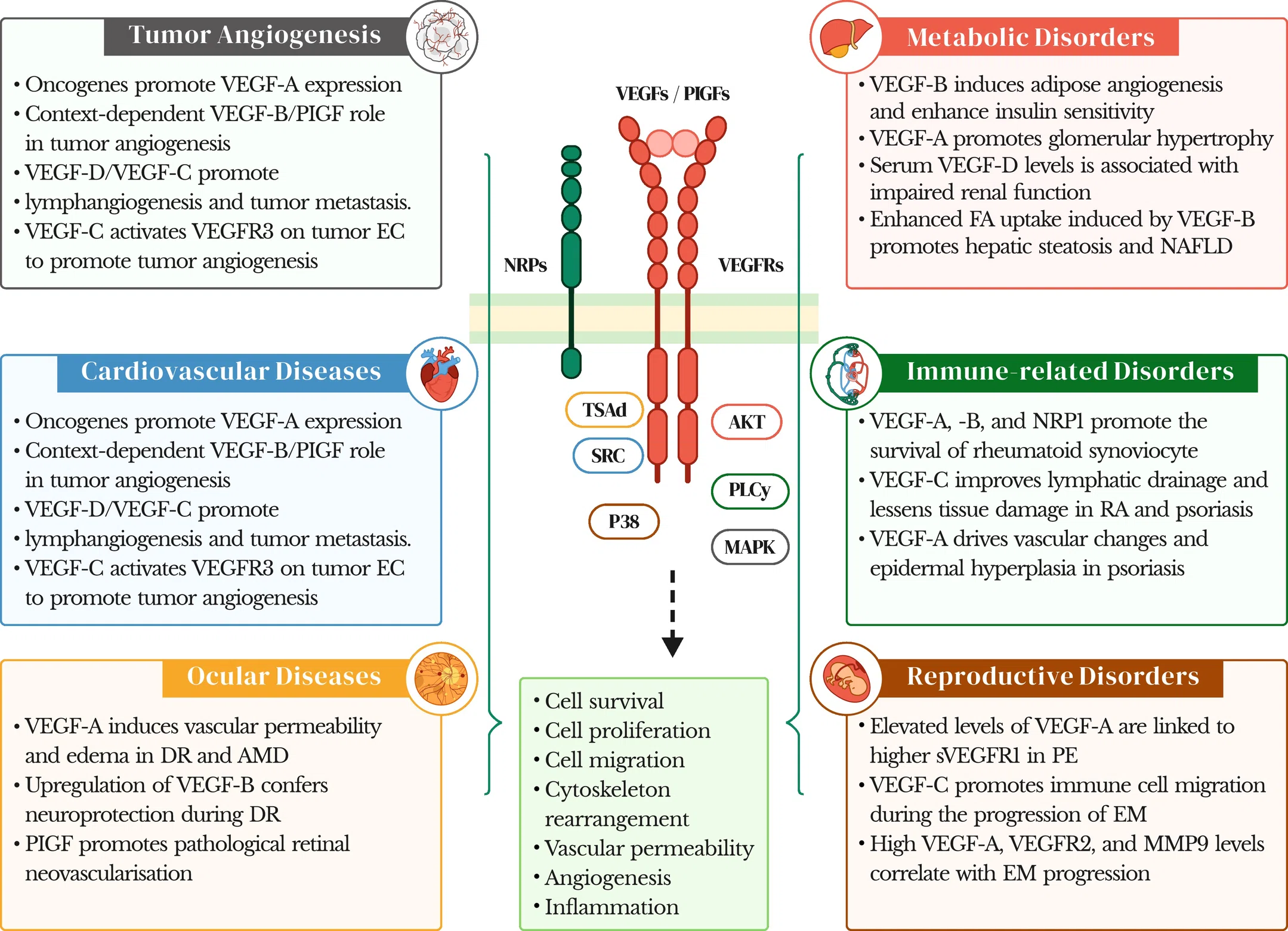
VEGF信号通路与疾病
然而,当VEGF信号活性异常时,会打破这一平衡:活性过高常常会促进肿瘤生长、侵袭和转移,而信号传导不足则会导致伤口愈合障碍和缺血性疾病。
研究表明,关键分子相互作用及下游信号通路在病理状态下呈现上调或失调状态,会促进细胞存活、迁移与增殖,从而导致ATH(动脉粥样硬化)、MI(心肌梗死)、DR(糖尿病视网膜病变)、AMD(年龄相关性黄斑变性)、FA(脂肪酸)等疾病的发生和发展,这些疾病背景凸显了靶向VEGF信号通路的治疗潜力。
04
治疗策略及临床应用
目前,针对VEGF信号的靶向疗法已成为肿瘤和眼科领域的里程碑:
l 配体中和:贝伐珠单抗(Bevacizumab)是人源化抗VEGF-A单抗,已获批用于结直肠癌、肺癌等多种实体瘤;雷珠单抗(Ranibizumab)和阿柏西普(Aflibercept,VEGF-trap)用于湿性AMD和DR。
l 受体抑制:雷莫芦单抗(Ramucirumab,抗VEGFR-2单抗)和多靶点酪氨酸激酶抑制剂(如索拉非尼、舒尼替尼)阻断下游信号。
l 新兴策略:双靶点药物(如faricimab,同时抑制VEGF和Ang-2)、联合免疫检查点抑制剂、PROTAC降解剂和基因/ siRNA疗法正在克服耐药和副作用(如高血压、蛋白尿)。
这些疗法通过“血管正常化”改善药物递送,并与化疗、免疫疗法协同。未来,个性化治疗和多通路联合将成为趋势。
利用基因敲除细胞模型,可深入探究VEGF家族成员在不同疾病中的调控机制,推动新药研发与疾病治疗策略的突破。
艾迪基因现已推出VEGF通路系列产品,为疾病机制研究、肿瘤靶向疗法的探索提供稳定可靠的研究工具。
FAQ
我想研究VEGF在特定癌症(如胶质母细胞瘤)中的作用,但列表里没有这种细胞。
我们提供定制服务。您可提供目标细胞系,我们为您完成从基因编辑到单克隆验证的全流程。同时,您可先用HEK293或HeLa中的通用模型进行预实验,验证您的科学假设。
这些细胞能否用于体内实验?
当然可以。许多客户将我们的VEGFA-KO或VEGFR2-KO的肿瘤细胞系接种于小鼠,用于研究基因缺失对体内成瘤、血管生成及转移的影响。
我计划做一个高通量药物筛选,需要大量同批次的细胞,可以满足吗?
可以。我们所有现货细胞均有主细胞库和工作细胞库系统,可为您提供大量、批次稳定的细胞,确保您筛选数据的均一性与可比性。
参考文献
1. Lee, C., Kim, M. J., Kumar, A., Lee, H.-W., Yang, Y., & Kim, Y. (2025). Vascular endothelial growth factor signaling in health and disease: From molecular mechanisms to therapeutic perspectives. Signal Transduction and Targeted Therapy, 10(1), Article 170. https://doi.org/10.1038/s41392-025-02249-0
2. Shah, F. H., Nam, Y. S., Bang, J. Y., Hwang, I. S., Kim, D. H., Ki, M., & Lee, H. W. (2025). Targeting vascular endothelial growth receptor-2 (VEGFR-2): Structural biology, functional insights, and therapeutic resistance. Archives of Pharmacal Research, 48(5), 404–425. https://doi.org/10.1007/s12272-025-01545-1
3. Li, H. S., & Huang, X. G. (2025). Advances in the molecular signaling mechanisms of VEGF/VEGFR2 in fundus neovascularization disease (Review). Experimental and Therapeutic Medicine, 30, 143. https://doi.org/10.3892/etm.2025.12893
4. Liu, Y., Li, Y., Wang, Y., Lin, C., Zhang, D., Chen, J., Ouyang, L., Wu, F., Zhang, J., & Chen, L. (2022). Recent progress on vascular endothelial growth factor receptor inhibitors with dual targeting capabilities for tumor therapy. Journal of Hematology & Oncology, 15(1), Article 89. https://doi.org/10.1186/s13045-022-01310-7

2. Shah, F. H., Nam, Y. S., Bang, J. Y., Hwang, I. S., Kim, D. H., Ki, M., & Lee, H. W. (2025). Targeting vascular endothelial growth receptor-2 (VEGFR-2): Structural biology, functional insights, and therapeutic resistance. Archives of Pharmacal Research, 48(5), 404–425. https://doi.org/10.1007/s12272-025-01545-1
3. Li, H. S., & Huang, X. G. (2025). Advances in the molecular signaling mechanisms of VEGF/VEGFR2 in fundus neovascularization disease (Review). Experimental and Therapeutic Medicine, 30, 143. https://doi.org/10.3892/etm.2025.12893
4. Liu, Y., Li, Y., Wang, Y., Lin, C., Zhang, D., Chen, J., Ouyang, L., Wu, F., Zhang, J., & Chen, L. (2022). Recent progress on vascular endothelial growth factor receptor inhibitors with dual targeting capabilities for tumor therapy. Journal of Hematology & Oncology, 15(1), Article 89. https://doi.org/10.1186/s13045-022-01310-7

联系我们
18102225074(微信同号)market@edgene.cn












